Le citrate de tofacitinib est un médicament sur ordonnance (nom commercial Xeljanz) développé à l'origine par Pfizer pour une classe d'inhibiteurs oraux de la Janus kinase (JAK). Il peut inhiber sélectivement la JAK kinase, bloquer les voies JAK/STAT et ainsi inhiber la transduction du signal cellulaire ainsi que l'expression et l'activation des gènes associés, utilisés pour traiter la polyarthrite rhumatoïde, l'arthrite psoriasique, la colite ulcéreuse et d'autres maladies immunitaires.
Le médicament comprend trois formes posologiques : comprimés, comprimés à libération prolongée et solutions buvables. Ses comprimés ont été approuvés pour la première fois par la FDA en 2012, et la forme posologique à libération prolongée a été approuvée par la FDA en février 2016. Il s'agit de la première à traiter les articulations rhumatoïdes. Yan est un inhibiteur de JAK pris par voie orale une fois par jour. En décembre 2019, une nouvelle indication de médicaments à libération prolongée a de nouveau été approuvée pour le traitement de la colite ulcéreuse (CU) active modérée à sévère. De plus, les essais cliniques de phase 3 en cours sur le psoriasis en plaques sont terminés et six autres essais cliniques de phase 3 sont en cours, impliquant le rhumatisme psoriasique actif, l'arthrite juvénile idiopathique, etc. Les avantages des comprimés à libération prolongée, à action prolongée et à prendre seulement une fois par jour, sont propices à la gestion et au contrôle des maladies des patients.
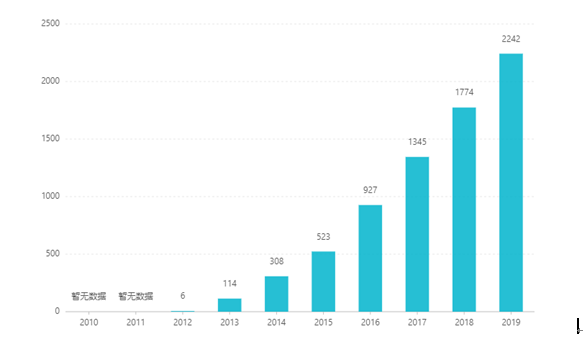
Depuis son introduction en bourse, ses ventes ont augmenté d'année en année, atteignant 2,242 milliards de dollars américains en 2019. En Chine, la forme posologique en comprimés a été approuvée pour la commercialisation en mars 2017 et est entrée dans le catalogue de l'assurance médicale de catégorie B grâce à des négociations en 2019. Le dernier gagnant l'offre est de 26,79 RMB. Cependant, en raison des barrières techniques élevées des préparations à libération prolongée, cette forme galénique n'a pas encore été commercialisée en Chine.
La JAK kinase joue un rôle important dans l’inflammation et il a été démontré que ses inhibiteurs traitent certaines maladies inflammatoires et auto-immunes. Jusqu'à présent, 7 inhibiteurs de JAK ont été approuvés dans le monde, dont le Delgocitinib de Leo Pharma, le Fedratinib de Celgene, l'upatinib d'AbbVie, le Pefitinib d'Astellas, le Baritinib d'Eli Lilly et le Rocotinib de Novartis. Cependant, seuls le tofacitinib, le baritinib et le rocotinib sont approuvés en Chine parmi les médicaments mentionnés ci-dessus. Nous attendons avec impatience que les « comprimés à libération prolongée de citrate de tofatib » de Qilu soient approuvés dès que possible et profitent à davantage de patients.
En Chine, la recherche originale sur le citrate de tofacitib a été approuvée par la NMPA en mars 2017 pour le traitement des patients adultes atteints de PR présentant une efficacité insuffisante ou une intolérance au méthotrexate, sous le nom commercial Shangjie. Selon les données de Meinenet, les ventes de comprimés de citrate de tofacitib dans les institutions médicales publiques chinoises en 2018 s'élevaient à 8,34 millions de yuans, ce qui était bien inférieur aux ventes mondiales. Une grande partie de la raison est le prix. Il est rapporté que le prix de détail initial de Shangjie était de 2 085 yuans (5 mg * 28 comprimés) et que le coût mensuel était de 4 170 yuans, ce qui n'est pas un petit fardeau pour les familles ordinaires.
Cependant, il convient de célébrer que le tofacitib ait été inclus dans la « Liste nationale des médicaments de l'assurance maladie de base, de l'assurance contre les accidents du travail et de l'assurance maternité » de 2019 par l'Administration nationale de l'assurance maladie après des négociations en novembre 2019. Il est rapporté que les frais mensuels seront réduits. à moins de 2 000 yuans après la négociation de la baisse de prix, ce qui améliorera considérablement la disponibilité du médicament.
En août 2018, le Conseil de réexamen des brevets de l'Office national de la propriété intellectuelle a rendu une décision de révision n° 36902, demande d'invalidation, et a déclaré invalide le brevet principal du Pfizertofatib, le brevet composé, au motif d'une divulgation insuffisante de la spécification. Cependant, le brevet sur la forme cristalline du Pfizertofatiib (ZL02823587.8, CN1325498C, date de demande 2002.11.25) expirera en 2022.
La base de données Insight montre qu'en plus de la recherche originale, cinq médicaments génériques de Chia Tai Tianqing, Qilu, Kelun, Yangtze River et Nanjing Chia Tai Tianqing ont été approuvés pour la commercialisation dans les formulations nationales de comprimés de tofacitinib. Cependant, pour le type de comprimé à libération prolongée, seule la recherche originale Pfizer a soumis une demande de commercialisation le 26 mai. Qilu est la première entreprise nationale à soumettre une demande de commercialisation pour cette formulation. Par ailleurs, le CSPC Ouyi est en phase de procès BE.
Changzhou Pharmaceutical Factory (CPF) est l'un des principaux fabricants pharmaceutiques d'API et de formulations finies en Chine, situé à Changzhou, dans la province du Jiangsu. CPF a été fondée en 1949. Nous nous sommes consacrés au citrate de tofacitinib à partir de 2013 et avons déjà soumis du DMF. Nous nous sommes enregistrés dans de nombreux pays et pouvons vous aider avec les meilleurs documents d'assistance pour le citrate de tofacitinib.
Heure de publication : 23 juillet 2021