Mésylate de dabigatran etexilate
Description
Le mésylate d'étéxilate de dabigatran (BIBR 1048MS) est un promédicament oralement actif du dabigatran. Le mésylate de dabigatran etexilate a des effets anticoagulants et est utilisé pour la prophylaxie de la thromboembolie veineuse et des accidents vasculaires cérébraux dus à la fibrillation auriculaire.
Arrière-plan
Description : Valeur IC50 : 4,5 nM (Ki) ; 10 nM (agrégation plaquettaire induite par la thrombine) [1] Le dabigatran est un inhibiteur direct de la thrombine (DTI) réversible et sélectif en cours de développement clinique avancé en tant que promédicament oral actif, le dabigatran etexilate. in vitro : le dabigatran a inhibé de manière sélective et réversible la thrombine humaine (Ki : 4,5 nM) ainsi que l'agrégation plaquettaire induite par la thrombine (IC(50 : 10 nM), tout en ne montrant aucun effet inhibiteur sur d'autres agents stimulant les plaquettes. Génération de thrombine dans les plaquettes -un plasma pauvre (PPP), mesuré par l'inhibition du potentiel de thrombine endogène (ETP) de manière dépendante de la concentration (IC (50) : 0,56 microM). Le dabigatran a démontré des effets anticoagulants dépendants de la concentration chez diverses espèces in vitro, doublant le temps de céphaline activée (aPTT), le temps de prothrombine (PT) et le temps de coagulation de l'écarine (ECT) dans le PPP humain à des concentrations de 0,23, 0,83 et 0,18 microM, respectivement. 1]. in vivo : le dabigatran a prolongé l'aPTT de manière dose-dépendante après administration intraveineuse chez le rat (0,3, 1 et 3 mg/kg) et le singe rhésus (0,15, 0,3 et 0,6 mg/kg). Des effets anticoagulants dépendants de la dose et du temps ont été observés avec le dabigatran etexilate administré par voie orale à des rats conscients (10, 20 et 50 mg/kg) ou à des singes rhésus (1, 2,5 ou 5 mg/kg), avec des effets maximaux observés entre 30 et 120 mg/kg. min après l'administration, respectivement [1]. Les patients traités par dabigatran etexilate ont présenté moins d’accidents vasculaires cérébraux ischémiques (3,74 dabigatran etexilate vs 3,97 warfarine) et moins d’hémorragies intracrâniennes et d’accidents vasculaires cérébraux hémorragiques combinés (0,43 dabigatran etexilate vs 0,99 warfarine) pour 100 années-patients [2]. Essai clinique : une évaluation de la pharmacocinétique et de la pharmacodynamique du dabigatran étexilate oral chez les patients hémodialysés. Phase1
Stockage
| Poudre | -20°C | 3 ans |
| 4°C | 2 ans | |
| En solvant | -80°C | 6 mois |
| -20°C | 1 mois |
Essai clinique
| Numéro NCT | Parrainer | Condition | Date de début | Phase |
| NCT02170792 | Boehringer Ingelheim | En bonne santé | Février 2001 | Phase 1 |
| NCT02170974 | Boehringer Ingelheim | En bonne santé | juillet 2004 | Phase 1 |
| NCT02170831 | Boehringer Ingelheim | En bonne santé | mai 1999 | Phase 1 |
| NCT02170805 | Boehringer Ingelheim | En bonne santé | avril 2001 | Phase 1 |
| NCT02170610 | Boehringer Ingelheim | En bonne santé | Mars 2002 | Phase 1 |
| NCT02170909 | Boehringer Ingelheim | En bonne santé | décembre 2004 | Phase 1 |
| NCT02171000 | Boehringer Ingelheim | En bonne santé | avril 2005 | Phase 1 |
| NCT02170844 | Boehringer Ingelheim | En bonne santé | juin 2004 | Phase 1 |
| NCT02170584 | Boehringer Ingelheim | En bonne santé | janvier 2001 | Phase 1 |
| NCT02170935 | Boehringer Ingelheim | Thromboembolie veineuse | avril 2002 | Phase 2 |
| NCT02170636 | Boehringer Ingelheim | En bonne santé | janvier 2002 | Phase 1 |
| NCT02170766 | Boehringer Ingelheim | En bonne santé | Octobre 2000 | Phase 1 |
| NCT02171442 | Boehringer Ingelheim | En bonne santé | avril 2002 | Phase 1 |
| NCT02170896 | Boehringer Ingelheim | En bonne santé | Octobre 2001 | Phase 1 |
| NCT02173730 | Boehringer Ingelheim | En bonne santé | novembre 2002 | Phase 1 |
| NCT02170623 | Boehringer Ingelheim | En bonne santé | Février 2002 | Phase 1 |
| NCT02170116 | Boehringer Ingelheim | En bonne santé | Novembre 1998 | Phase 1 |
| NCT02170597 | Boehringer Ingelheim | En bonne santé | Août 2003 | Phase 1 |
| NCT01225822 | Boehringer Ingelheim | Thromboembolie veineuse | novembre 2002 | Phase 2 |
| NCT02170701 | Boehringer Ingelheim | Thromboembolie veineuse | Octobre 2000 | Phase 2 |
| NCT02170740 | Boehringer Ingelheim | En bonne santé | Novembre 1999 | Phase 1 |
| NCT02170922 | Boehringer Ingelheim | En bonne santé | juillet 1999 | Phase 1 |
Structure chimique
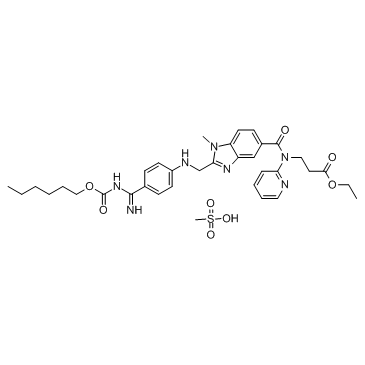





Proposition18Projets d'évaluation de la cohérence de la qualité qui ont été approuvés4, et6les projets sont en cours d’approbation.

Un système international avancé de gestion de la qualité a jeté des bases solides pour les ventes.

La supervision de la qualité s'étend tout au long du cycle de vie du produit pour garantir la qualité et l'effet thérapeutique.

L’équipe professionnelle des affaires réglementaires répond aux exigences de qualité lors de la demande et de l’enregistrement.


Ligne d'emballage en bouteille Korea Countec


Ligne d'emballage en bouteille CVC de Taiwan


Ligne d'emballage de carton CAM Italie

Machine de compactage allemande Fette

Détecteur de comprimés Viswill du Japon

Salle de contrôle DCS







